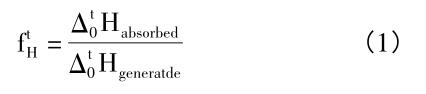引言
锆及锆合金由于具有极低的热中子吸收截面、高温下优异的耐腐蚀性能以及与 UO2核燃料良好的兼容性,因此被广泛应用于核工业结构部件,比如核燃料包壳管、压力管中及反应堆栅格,对核反应系统的安全性起着第一道屏障的作用。然而在核反应堆运行过程中,其长期处于高温、高压及强辐照的服役环境下,高温的水与锆合金发生缓慢的水侧均匀腐蚀 ,Zr + 2H2O→ZrO2 + 2H2。在核燃料包壳管表面形成以单斜 ZrO2为主的氧化层,氧化层的最大厚度可达 100 μm[1],并在腐蚀过程中伴随有氢气的生成。腐蚀初始阶段氧化膜层黑亮且致密,对内基体起一定的延缓氧化及阻挡氢气吸收的作用。然而随着堆内运行周期的延长,当膜层生长到一定厚度后会发生开裂及剥落现象,裂纹为氢气的入侵起到快速通道的作用,加快锆基体在高温下的氢气吸收速率。氢含量较少时,氢在锆合金中优先占据四面体间隙位置,形成间隙固溶体[2],当氢含量达到固溶极限后则会在基体中析出氢化物即氢化锆。氢化锆是一种脆性相,拉伸试验表明,其在室温至 600 ℃之间的延伸率几乎为零[3]。此外,在氢化锆形成过程中伴随着体积的增大,引起周围基体晶格畸变,因此很容易导致锆合金基体微裂纹的产生,形成氢致延迟开裂。氢化与氧化交互作用,造成核燃料包壳管的失效,对核反应堆的正常运行产生严重的安全隐患。
目前对于核电站的研究逐步向着高燃耗、高安全性及低消耗的趋势发展,燃料棒的燃耗可由30GWd/tMH 提高至 50 GWd /tMH,核燃料包壳管在堆内的服役时间由 3 年增加至 5 年[4],这对其使用性能提出了更高的要求,而吸氢导致的氢脆问题严重制约了锆合金包壳管的使用寿命。基于此问题,近 60 年来,国内外对氢化物的形成机制、组织形貌及力学性能进行了大量的研究。本文对此前的研究进行了归纳综述,以期为国内相关工作的开展提供参考和建议。
1、氢化物的形成
1.1氢的吸收
锆合金包壳管吸氢的来源主要有:(1) 腐蚀反应过程产生的氢;(2) 一回路冷却水和蒸汽中溶解的氢;(3)由于中子辐照效应水分解产生的氢,然而在研究工作中通常只考虑腐蚀反应过程产生的氢[5]。因此可以推断氢的吸收量与腐蚀速率和腐蚀阶段有着密切的关系。为了便于表述锆合金在腐蚀过程中的吸氢性能,通常采用公式(1)来进行说明[6]。
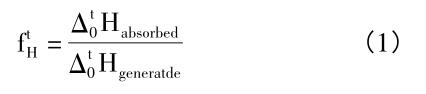
式中Δt0 Habsorbed 表示氢的吸收量,Δt0 Hgenerate 表示腐蚀过程产生氢的总量。Couent[6]在高压釜中模拟核反应堆运行环境进行腐蚀试验并研究了锆合金中氢含量与腐蚀程度之间的关系,见图 1。
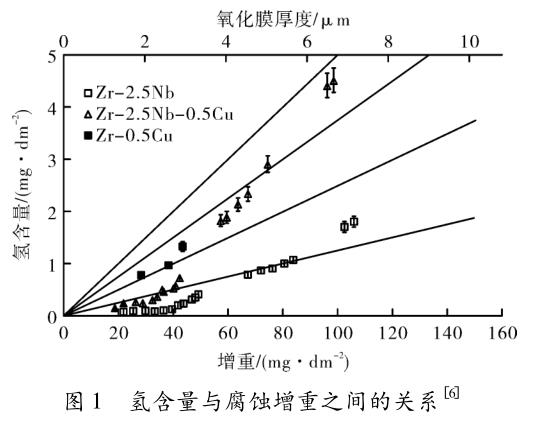
图 1 表示腐蚀增重( 以腐蚀增重代表腐蚀程度)与吸氢量之间的关系,通常认为吸氢分数为常数。假如吸氢分数为恒定值,那么氢含量与腐蚀增重之间应呈线性函数关系,如图 1 中虚直线所示。
从图 1 可以看出,实际腐蚀过程中氢含量与腐蚀增重之间呈现类似抛物线的函数关系而不是线性的,随着腐蚀时间的延长,氢的吸收速率加快即吸氢分数增大。虽然在试验过程中氧化膜层没有宏观裂纹及脱落现象,然而锆的 P.B( Piuing-Bedworth) 比为1.56,即在氧化过程中会发生体积膨胀,基体内部会形成内应力与微观缺陷比如位错和空位等。当内应力场与氢的应变场交互作用时,氢容易被吸引到缺陷位置附近,形成氢陷阱,且由位错中心所引起的晶格畸变比间隙氧原子产生的畸变大,因此位错同氢的交互作用更加强烈[7]。随着腐蚀程度的加剧,位错密度增大,氢吸收速率加快。此外,3 种锆合金的吸氢速率有明显的差别,可推断合金元素对氢的吸收有重要的影响,添加元素 Nb 有助于抑制氢的吸收,而 Cu 元素会促进氢的吸收。此研究为锆合金在腐蚀初期阶段的吸氢性能,而通常包壳管在堆内的服役时间为 3 ~ 5 年,因此需要开展更多的相关试验来研究长期腐蚀以及合金元素对锆合金吸氢性能的影响。
1.2锆合金基体中氢的固溶度
被吸收的氢首先占据密排六方结构 α-Zr 的四面体间隙位置形成间隙固溶体,且固溶体中氢的固溶度受诸多因素的影响。1968 年 Ells[8]研究发现锆合金中氢的固溶度受温度影响变化较大,在室温下约为 1 × 10-6,在573 K 为 70 × 10-6,而在 773 K 则升高至 500 ×10-6。近年来关于温度对固溶度的影响也有一些报道。S.Suman[9]采用 3D 仿真模拟结合有限元的方法分析氢化物对裂纹扩展的影响时发现,在 573 K时氢的固溶度为 80 × 10-6,在 673 K 时约为 200 ×10-6。K.Une[10]对氢原子在 Zr-2 合金中的扩散进行物理建模并采用差示扫描量热法(DSC)对氢浓度随温度的变化进行测量,发现在室温下氢的固溶度为 1 × 10-6,在 573 K 为 150 × 10-6,773 K 时达到560 × 10-6。
由上述研究成果可知随着温度的升高,氢的固溶度逐渐增大,这可能是由于温度越高,原子热振动越激烈,使得处于间隙位置的氢原子获得足够的能量发生间隙扩散和空位扩散。
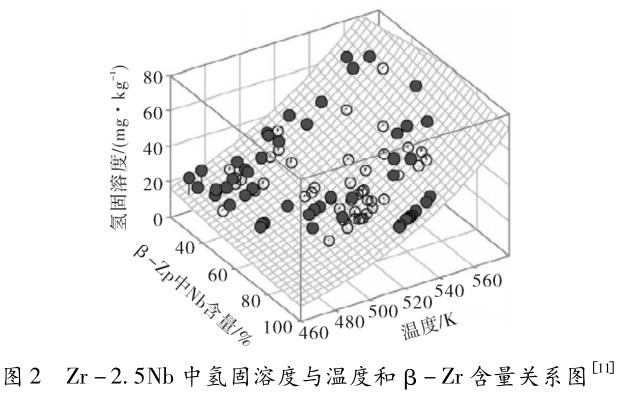
D.Khatamian[11]采用 DSC 和真空热抽取气相色谱法研究了 β-Zr 相对氢固溶度的影响,并对数据进 行 拟 合,结 果 见 图 2。 试 样 为 挤 压 态 的Zr-2.5Nb管材,管材中含有一定量的 β-Zr。由于β-Zr 在 900 K 以下为亚稳相,会发生共析转变生成 α-Zr 和 β-Nb[12],因此可以用 β 相中 Nb 的含量来表示 β-Zr 的分解程度。图 2 中三维网面代表理论计算得到的固溶度,黑球和白球分别代表处于网面以上和网面以下的数据集。从图 2 可以看出,试验数据和理论计算值拟合良好,温度和 β 相的含量均对氢固溶度有一定的影响,随着 β 相的减少,氢固溶度逐渐减小,当 β 相完全分解时,固溶度达到最小值。此外,固溶度还受应力场的影响。锆合金中的氢是高度流动的,当合金中的应力分布不均匀时,会形成一定的应力梯度,这成为氢扩散的驱动力,使得氢原子向张应力大的方向移动[13]。
当合金中的氢含量超过固溶极限时氢化物会优先在与惯习面方向一致的晶界处析出[14,15]。因此晶界的取向对于氢化物的形成也有重要的影响。Mani Krishna[16]使用重位点阵(CSL)物理模型对氢化物的生长进行模拟,发现当锆合金中 α 相与 β 相共存时,氢化物优先在 α-β 相界面处形核并生长。
2、氢化物的分类
2.1根据氢含量的分类
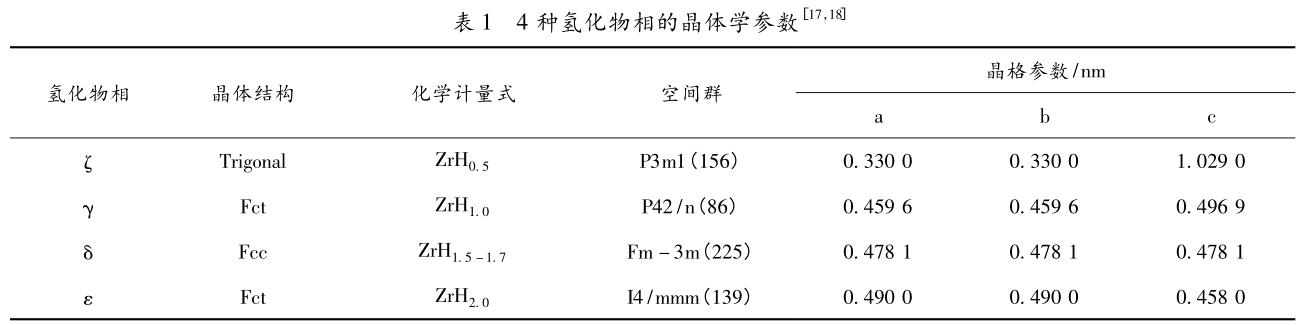
根据氢含量及晶体结构,锆合金中的氢化物可分为 4 类,即 ζ、γ、δ 和 ε 相,具体晶体学参数见表 1。
2.1.1ζ 相
锆合金中 γ、δ 和 ε 相氢化物存在比较广泛,通过试验手段也较易制备,从 20 世纪 50 年代开始研究人员对这 3 种氢化物进行了广泛的研究。
1963 年,Bailey.J[18]在报道中提到除了 3 种常见的氢化物相之外,应该还存在第四种氢化物 ζ 相。直到 2008 年 Zhao[19]等通过试验确定了 ζ 相的存在,认为 ζ 相是介于 α-Zr 与 γ/δ 相之间的过渡相,属于亚稳相,并借助 TEM 旋进电子衍射和第一性原理的方法得出其晶体结构、空间点群和晶格常数等信息。至今关于 ζ 相的热力学稳定性、形成方式及力学性能方面仍存在较多的争议。在 Zhao 的研究基础上,L.Thuinet[20]认为随着氢含量的增多 ζ 相会优先转变为与 α 锆基体共存的 γ 相,并提出了两种不同的转变方式:(1)α-Zr→ζ→fct-ζ→γ,(2)α -Zr→ζ→hcp-γ→γ。Zhang[21]通过热力学计算对这两种转变方式进行了理论验证,发现在核燃料包壳管服役温度下,第二种转变方式中由 hcp-γ 相转变为 γ 相需要克服的势垒非常大,转变难以进行,而相较于第二种,第一种转变方式在剪切滑移转变过程中需要克服的势垒非常小,因此推测在一定的温度下 ζ 氢化物相会以第二种方式转变为 γ 型氢化物相。Zhu[22]等使用 Basin-Hopping 算法进行高效结构搜索发现 ζ-ZrH0.5 存在另外两种隶属三方晶系的晶体结构。一种是 R 3- m 对称点群的晶体结构,另外一种与 Zhao 的研究结果一致,同样属于 p3m1对称点群的晶体结构,但氢原子在晶胞中的位置不同,通过第一性原理对其能量进行计算,新发现的p3m1 ζ-ZrH0.5能量很低,具有较好的动态稳定性和力学稳定性。
2.1.2γ 相与 δ 相
自 20 世纪 60 年代以来关于 γ-ZrH 是否为稳定相还一直存在争议,并且一些早期的二元相图中并不包含 γ 相[23]。大多数的研究报道认为 γ 相是一种亚稳相,只有在特定条件下才能稳定存在[24]。Besson 运用从头算方法对 γ 氢化物的热力学稳定性进行计算,发现 γ 相在低温时为亚稳相,而当温度升高至 500 K 时转变为稳定相[25]。然而 Ma[26]和Kim[27]在接下来的试验中却发现室温条件下氢化物中含有稳定存在的 γ 相。笔者认为,γ 氢化物能否稳定存在受诸多因素的影响,比如晶体中的内应力、外在施加应力、合金元素等,而温度只是诸多因素中比较重要的一个,这需要更多的理论和试验来进行验证。
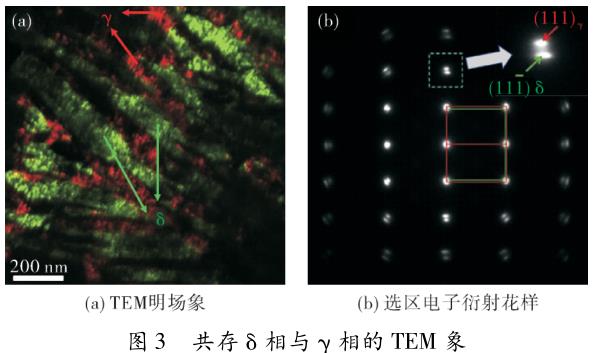
氢化物的相变主要以马氏体转变的方式进行,在大量 δ 相形成的过程中往往会有少量的 γ 相共存,两者均为细小的层片状显微形貌,见图 3(a)(红色代表 γ 相,绿色代表 δ 相),且 γ 相与 δ 相的晶格常数非常相似,因此在衍射花样标定过程中会出现衍射斑类似重合的现象,见图 3(b)。研究者对 γ 相与 δ 相的形成条件也进行了一些研究,普遍认为氢化过程中的冷却速率起决定性作用。当快速冷却时主要形成 γ 相氢化物,冷却速率较慢时主要为 δ 相氢化物[28-30]。最近,Kim[27]在试验中通过0.5 K/min的冷却速率得到了纯净的 δ 相氢化物,当冷却速率提高至 300 K/min 时得到了 γ 相与 δ 相共存的氢化物,这也证实了上述论点。然而,Cann[31]通过试验发现 γ 相与 δ 相的形成与金属基体中的氧含量存在很大的关联,氧浓度较高时容易形成 δ 氢化物,反之则形成 γ 氢化物。在核反应堆运行过程中,冷却剂对锆合金燃料包壳的冷却速率相对较慢,往往会形成较多的 δ 氢化物,且研究表明,δ 相在形成过程中相对于锆合金基体 α 相产生较大的体积膨胀率(约 17% )[32],因此可推断 δ 相氢化物的形成是包壳管氢致延迟开裂(DHC)的主要原因。
2.1.3ε 相
在室温下当氢与锆的原子比超过 1.7 以上时会形成单一的 ε 氢化物相[33]。ε 相为畸变的萤石面心四方结构(fct),c /a ﹤ 1,且晶格参数随着成分的改变发生微小的变化[33]。通常 ε 氢化物为带状孪晶结构,相邻晶粒里的孪晶取向不同,且随着氢含量的增加,这种带状的孪晶结构特征越显著。孪晶界属于二维面缺陷,应力和吸收的氢容易在此聚集,当有 ε 氢化锆形成时,裂纹容易在孪晶界处萌生。在1 073 K 由 δ 向 ε 相转变时晶格常数变化很小,体积大约减小 4%[34],然而由于氢化锆本身属于脆性相,塑性较差,因此当有少量的内应力和应变存在时也会有大量的缺陷生成。
2.2介观尺度下氢化物的分类
氢化物在析出的初始阶段为独立的纳米尺寸的小颗粒,由于受到金属基体的制约,在氢化物的生长过程中会产生弹性应变场,受到应力作用的氢化物优先在初始氢化物周围形核,经过反复形核与连续生长,聚集形成介观尺度的氢化物团簇。氢化物根据在介观尺度下的形态可分为边缘氢化物和泡状氢化物。
2.2.1边缘氢化物
反应堆运行过程中,热量由核燃料包壳管内向管外传递,形成稳定的热流及由内至外的温度梯度,成为氢扩散的驱动力。被锆合金吸收的氢受到温度梯度的影响发生非稳态扩散,由温度高的区域(内壁)流向温度低的区域(外壁)导致氢在包壳管外表面聚集,形成边缘氢化物[35],见图 4。

Kim[36]等对含有边缘氢化物的 Zr-4 包壳管进行环向拉伸试验,经研究发现管材的塑性随着边缘氢化物厚度的增加而降低,且在断裂过程中,边缘氢化物能为裂纹提供扩展通道,加速管材的断裂。图 4(a)中氢化物沿周向分布,(b)中氢化物沿径向分布。经研究表明,氢化物的取向与锆合金包壳管的加工参数 Q 密切相关,Q 为管壁变形量与管径变形量的比值[38]。当 Q 值较大时即加工过程以减壁为主,管材内部会产生沿轴向的压应力和沿切向的张应力,当合金中存在内应力时氢化物平行于压应力而垂直于张应力析出,进而形成周向分布的氢化物,反之,当 Q 值较小时则形成沿径向分布的氢化物。通常认为,径向氢化物对锆合金管材的塑性影响较大,沿周向分布时影响较小。Kim[39]研究发现,当 Zr-4 包壳管中氢含量达到 826 × 10-6时,合金基体析出大量的周向氢化物,在室温下管材呈现完全脆性,温度达到 423 K 时可以发生较大的塑性变形,恢复塑性,然而当氢化物呈径向分布时,即使氢含量为 100 × 10-6 ~ 150 × 10-6,在 423 K 仍表现为脆性相。Min[40]等研究发现,当管材中同时存在径向氢化物与周向氢化物时,微裂纹优先在径向氢化物处萌生,并沿着与之相结临的径向氢化物扩展,形成脆性断裂。在没有相互连接的径向氢化物时,微裂纹会向邻近的周向氢化物扩展,产生韧性断裂。核燃料包壳管在长期服役过程中会不可避免的吸氢生成氢化物,为了使氢化物对包壳管的不利影响最小化,在实际的包壳管加工过程中,应严格控制轧制工艺,以确保析出的氢化物沿周向分布。
2.2.2泡状氢化物
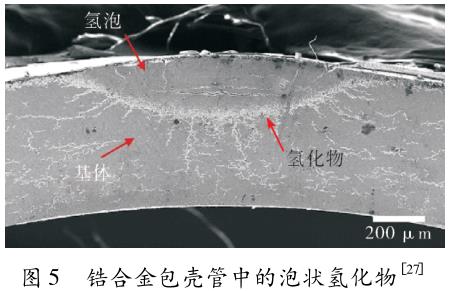
核燃料包壳管在水侧腐蚀反应的初期,外表面会形成很薄的氧化膜,当膜层生长到一定厚度时会发生破裂并局部脱落,在管材表面形成冷斑。被吸收的氢受温度梯度的影响由温度高的区域移动到温度低的区域,导致氢在冷斑处大量聚集,析出氢含量极高的泡状氢化物(也称为太阳状氢化物)[41],简称氢泡,见图 5。1983 年 Pickering 二号核反应堆发生故障,经调查事故原因是氢泡在氢致延迟开裂的作用下导致了压力管的破裂,事件之后研究人员对氢泡进行了一些理论和试验研究。
在试验条件下可以通过镀 Ni 的方法来制备泡状氢化物,由于 Ni 具有强烈的吸氢性能,镀 Ni 的局部区域会大量吸氢并析出氢化物,进而形成氢泡。
相对于基材表面,氢泡会造成一定程度的凸起,Hel-louin[4 2]研究发现,凸起高度大约为氢泡总深度的22% ,因此可以根据凸起高度来估算氢泡延伸入锆合金基体的总深度。从图 5 可以看出氢泡呈椭球形,球体边缘的氢化物沿球体中心方向物呈辐射状分布,而 距 离 球 体 较 远 的 氢 化 物 沿 周 向 分 布。Singh[43]对此现象进行了研究,氢泡形成的初始阶段锆合金基体中的氢化物均呈周向分布,氢泡生长发生体积膨胀导致锆合金基体产生两种应力,即局部应力和总应力。局部应力是指周向氢化物板条间的压应力,该应力的分力 σ1 垂直于相邻的两个板条氢化物并影响氢化物的再取向。总应力是由于氢泡体积膨胀导致与合金基体发生体积失配而产生的应力,总应力的方向沿着球体中心与球面切线垂直,且与球体距离越近应力值越大。氢化物在两种应力的共同作用下发生应力再取向,当总应力处于主导地位且超过氢化物应力再取向阈值时,氢泡临近的周向氢化物发生应力再取向,形成辐射状分布。
Pierron[44]研究发现氢泡在 25 ~ 400 ℃ 之间均表现为脆性,当施加外在应力时,裂纹首先在氢泡中萌生,当氢泡下方的金属基材发生屈服现象后,裂纹以弹塑性断裂机制的方式迅速由氢泡向金属基体扩展。
3、结论
核能技术作为新能源的主要标志,因其不仅能替代一次性化石能源而且可以减轻环境污染的危害,近年来在世界范围内得到了愈来愈多的关注与发展。安全性是核工业发展最首要的问题,而对于整个核动力系统而言,最关键的部位是核反应堆堆芯,被锆合金包壳管包裹的 UO2芯块通过裂变向外界释放巨大的能量并产生大量辐射,因此对于锆合金作为结构材料的研究尤为重要。在堆内服役过程中锆合金包壳管吸氢并析出氢化物,这严重影响了合金基体的力学性能与包壳管的完整性,各国学者对此问题进行了大量的理论与试验研究,以下 3 个方面的问题有待继续深入研究:
(1)大部分的研究工作均在堆外进行并且模拟包壳管在堆内所面临的环境条件,比如温度、压力及水化学环境等,然而堆内的实际情况复杂得多,比如辐照肿胀、蠕变、PCI 等,这就造成试验数据与实际情况的偏差,因此采用计算机建模的方式进行数据处理与修正或许具有较大的研究价值。
(2)温度和氢含量对于锆合金基体的韧脆性转变具有很大的影响,然而学者对于这种转变发生的机理鲜有研究,此外,基体中由于体积失配引起的内应力、第二相粒子、辐照等对于韧脆性转变的影响也有待深入研究。
(3)目前商用的锆合金很多成分类似,且随着核反应堆向高燃耗的方向发展,很多传统的锆合金将面临淘汰,以往对于新锆合金的开发多采用“炒菜”式方式进行,随着计算机技术的发展,应当多采取计算机理论计算与实际实验相结合的方法研发新型锆合金。
参考文献
[1] Arthur T. Motta,Laurent Capolungo,Long-Qing Chen,et al. Hydrogen in zirconium alloys: A review[J]. Jour-nal of Nuclear Materials,2019,518(2-3):440-460.
[2]P A Burr,S T Murphy,S C Lumley,et al. Hydrogen solubility in zirconium intermetallic second phase particles [J]. Journal of Nuclear Materials,2013,443(1-3):502-506.
[3] W M Mueller,J P Blackledge,G G Libowitz. Metal Hy-drides [M],New York: Academic Press,1968: 312.
[4] J R Secker,B J Johansen,D L Stucker,et al. Optimum discharge burnup and cycle length for PWRs [J]. Nucle-ar Technology,2005,151(2): 109-119.
[5]刘建章. 核结构材料[M]. 北京:化学工业出版社,2007:144.
[6]A Couet,A T Motta,R J Comstock. Hydrogen pickup measurements in zirconium alloys: relation to oxidation kinetics [J]. Journal of Nuclear Materials,2014,451(1- 3): 1-13.
[7] B Cox. Hydrogen trapping by oxygen and dislocation zir-conium alloys [J]. Journal of Alloys and Compounds,1997,256(1-2): 4-7.
[8] C E Ells. Hydride precipitates in zirconium alloys (A re-view) [J]. Journal of Nuclear Materials. 1968,28(2):129-151.
[9] S Suman,M K Khan,M Pathak,et al. Hydrogen in zir-caloy: mechanism and its impacts [J]. Hydrogen Ener-gy,2015,40(17): 5 976-5 994.
[10]K Une,S Ishimoto,Y Etoh,et al. The terminal solid solubility of hydrogen in irradiated zircaloy-2 and mi-croscopic modeling of hydride behavior [J]. Journal of Nuclear Materials,2009,389(1): 127-136.
[11] D Khatamian. Effect of β-Zr decomposition on the sol-ubility limits for H in Zr-2. 5Nb[J]. Journal of Alloys and Compounds,2003,356-357(3): 22-26.
[12] B A Cheadle,S A Aldridge. The transformation and age hardening behaviour of Zr-19 wt% Nb [J]. Journal of Nuclear Materials,1973,47(2): 255-258.
[13] C J Simpson,C E Ells. Delayed hydrogen embrittlement in Zr-2. 5% Nb [J]. Journal of Nuclear Materials,1974,52 (2): 289-295.
[14]B Nath,G W Lorimer,N Ridley. Effect of hydrogen concentration and cooling rate on hydride precipitation in α zirconium [J]. Journal of Nuclear Materials,1975,58(2): 153-162.
[15] K Une,K Nogita,S Ishimoto,et al. Crystallography of zirconium hydrides in recrystallized zircaloy-2 fuel cladding by electron backscatter diffraction[J]. Journal of Nuclear Science & Technology,2004,41(7): 731 -740.
[16] K V M Krishna,A Sain,I Samajdar,et al. Resistance to hydride formation in zirconium: an emerging possibili-ty [J]. Acta Materialia,2006,54 (18): 4 665 -4 675.
[17] M P Puls. The effect of hydrogen and hydrides on the integrity of zirconium alloys compoments: delayed hy-drides cracking [M].Berlin: Springer Science and Business Media,2012: 112-113.
[18]J Bailey. Electron microscope observations on the pre-cipitation of zirconium hydride in zirconium[J]. Acta Metallurgica,1963,11(4): 267-280.
[19]Z Zhao,J P Morniroli,A Legris,et al. Identification and characterization of a new zirconium hydride [J].Journal of Microscopy,2008,232(3): 410-421.
[20] L Thuinet,R Besson. Ab initio study of competitive hy-dride formation in zirconium alloys [J]. Intermetallics,2012,20(1): 24-32.
[21] Y F Zhang,X M Bai,J Yu,et al. Homogeneous hy-dride formation path in α-Zr: molecular dynamics sim-ulations with the charge-optimized many-body poten-tial [J]. Acta Materialia,2016,111: 357-365.
[22] X Y Zhu,D Y Lin,J Fang,et al. Structure and ther-modynamic properties of zirconium hydrides by structure search method and first principles calculations [J].Computational Materials Science,2018,150(Part B):77-85.
[23] E Zuzek,J P Abriata. The H-Zr (hydrogen-zirconi-um) system [J]. Journal of Phase Equilibria,1990,11(4):385-395.
[24] L Lanzani,M Ruch. Comments on the stability of zirco-nium hydride phase in zirconium [J]. Journal of Nucle-ar Materials,2004,324(2-3): 165-176.
[25] R Besson,R Candela. Ab initio thermodynamics of fcc H-Zr and formation of hydrides [J]. Computational Materials Science,2016,114: 254-263.
[26] M W Ma,L Li,B H Tang,et al. Decomposition kinet-ics study of zirconium hydride by interrupted thermal de-sorption spectroscopy [J]. Journal of Alloys and Com-pounds,2015,645(1): 5217-5220.
[27] Sung-Dae Kim,Ju-Seong Kim,Jonhun Yoon. Phase analysis of hydride blister in zirconium alloy [J]. Jour-nal of Alloys and Compounds,2018,735 (5): 2007- 2011.
[28] Derek O Northwood,Daniel T H Lim. A TEM metallo-graphic study of hydrides in a Zr-2. 5 wt% Nb alloy [J]. Metallography,1981,14(1):21-35.
[29] J S Bradbrook,G W Lorimer,N Ridley. The precipitati-on of zirconium hydride in zirconium and zircaloy-2[J]. Journal of Nuclear Materials,1972,42(2): 142- 160.
[30] B Nath,G W Lorimer,N Ridley. The relationship be-tween γ and δ hydrides in zirconium-hydrogen alloys of low hydrogen concentration [J]. Journal of Nuclear Ma-terials,1973,49(3): 262-280.
[31] C D Cann,M P Puls,E E Sexton,et al. The effect of metallurgical factors on hydride phases in zirconium [J]. Journal of Nuclear Materials,1984,126(3): 197- 205.
[32] R N Singh,P Sthle,A R Massih,et al. Temperature dependence of misfit strains of δ-hydrides of zirconium [J]. Journal of Alloys and Compounds,2007,436(1- 2): 150-154.
[33]F A Lewis,A Aladjem.Hydrogen Metal Systems I [M]. Zurich: Scitec Publications,1996: 138-140.
[34]Hiroaki Muta,Ryoji Nishikane,Yusuke Ando,et al.Effect of hydrogenation conditions on the microstructure and mechanical properties of zirconium hydride [J].Journal of Nuclear Materials,2018,500: 145-152.
[35] R S Daum,S Majumdar,D W Bates,et al. On the em-brittlement of zircaloy-4 under RIA-relevant condi-tions [C]. West Conshohocken: ASTM International,2002: 702-718.
[36] Ju-Seong Kim,Ho-A Kim,So-Young Kang,et al.Effect of hydride rim on the ductility of zircaloy-4 clad-ding [J]. Journal of Nuclear Materials,2019,523:383-390.
[37] M C Billone,T A Burtseva,R E Einziger,Ductile-to- brittle transition temperature for high-burnup clad-ding alloys exposed to simulated drying storage condi-tions [J]. Journal of Nuclear Materials. 2013,433(1- 3): 431-448.
[38] G C Weatherly. The precipitation of γ-hydride plates in zirconium [J]. Acta Metallurgica,1981,29 (3):501-512.
[39]Ju-Seong Kim,Tae-Hoon Kim,Dong-Hak Kook,et al. Effect of hydride morphology on the embrittlement of Zircaloy-4 cladding [J]. Journal of Nuclear Materi-als,2015,456: 235-245.
[40]Su-Jeong Min,Myeong-Su Kim,Kyu-Tae Kim.Cooling rate and hydrogen content-dependent hydride reorientation and mechanical property degradation of Zr- Nb alloy claddings[J]. Journal of Nuclear materials,2013,441(1-3): 306-314.
[41] A M Garde,G P Smith,R C Pirek,Effects of hydride precipitate localization and neutron fluence on the ductil-ity of irradiated Zircaloy-4 [C]. Garmisch Parten-kirchen: ASTM STP,1996: 407-430.
[42]Arthur Hellouin de Menibus,Thomas Guibert,Quentin Auzoux,et al. Hydrogen contribution to the thermal ex-pansion of hydrided zircaloy-4 cladding tubes [J].Journal of Nuclear Materials,2013,440(1-3): 169 -177.
[43] R N Singh,R Kishore,T K Sinha,et al. Hydride blis-ter formation in Zr-2. 5Nb pressure tube alloy [J].Journal of Nuclear Materials,2002,301(2-3): 153 -164.
[44] O N Pierron,D A Koss,A T Motta,et al. The influ-ence of hydride blister on the fracture of zircaloy-4[J]. Journal of Nuclear Materials,2003,2(1): 21
相关链接